Pourquoi un lac gèle toujours par le dessus et autres petites leçons de physique autour de l’eau.
Il a neigé un peu partout en France. L’occasion de faire des batailles de boules de neige, des bonhommes avec de glorieuses carottes en guise d’appendice nasale ou simplement se promener.
L’auteur de cet article, en grand enfant, s’est promené cet après-midi autour du lac de Créteil et s’est posé une question toute bête mais qui mérite réponse : pourquoi les bords du lac étaient-ils encore gelés alors que l’intérieur était parfaitement liquide ?
L’occasion de faire un peu de vulgarisation scientifique à moindre frais !
Lire aussi :
- Découverte d’une nouvelle forme de glace qui bouleverse notre vision traditionnelle de l’eau
- Découverte d’une nouvelle forme pour l’eau en plus des états solide, liquide et gazeux qu’on pourrait rencontrer dans des océans extraterrestres
Réponses aux questions que vous vous êtes toujours posées (ou pas) sur le gel de l’eau
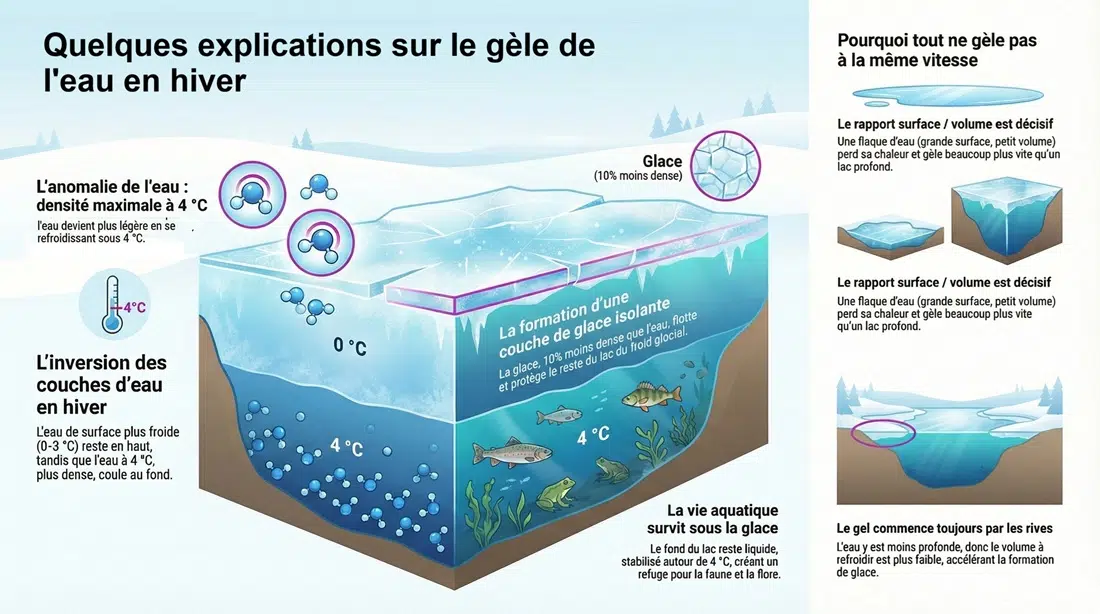
Pourquoi un lac gèle toujours par le dessus ?
En dessous de 0 °C, l’eau devient de la glace. Jusque-là, rien d’étonnant, vous connaissez la chanson. Ce qui l’est davantage, c’est que la glace est environ 10 % moins dense que l’eau liquide. Autrement dit, elle flotte. Cela explique à la fois pourquoi les glaçons montent dans un verre et pourquoi la banquise ne coule pas dans les océans.
La danse invisible des couches d’eau
Dans un lac, l’eau n’a jamais une température uniforme. Elle se range par couches, un peu comme une foule dans un amphithéâtre qui cherche instinctivement la meilleure place. Les eaux les plus denses descendent, les plus légères montent.
En été, lorsque l’air dépasse largement 4 °C, l’eau chaude en surface est aussi la moins dense. Elle flotte. L’eau plus froide, proche de 4 °C, se retrouve au fond. Les baigneurs connaissent bien cette sensation. Les pieds nagent dans une eau plus fraîche que la surface.
En hiver, tout s’inverse. L’air se refroidit sous 4 °C. L’eau de surface perd des degrés. En passant de 4 °C à 3 °C, elle devient moins dense. Elle remonte. L’eau légèrement plus chaude, autour de 4 °C, coule vers le fond. La stratification thermique se retourne complètement.
Ce mécanisme agit comme un tapis roulant thermique. Le fond du lac se stabilise autour de 4 °C, tandis que la surface continue à se refroidir jusqu’à atteindre 0 °C.
La glace naît là où l’air touche l’eau
Lorsque l’air reste durablement sous 0 °C, l’eau de surface finit par geler. Ce gel n’est pas un simple refroidissement. Il s’agit d’un changement d’état, gourmand en énergie.
Une fois formée, la glace reste en surface. Elle ne coule pas. Elle constitue même une barrière isolante entre l’air glacial et l’eau liquide située en dessous. Cette croûte protège littéralement le lac, un peu comme une couverture posée sur un corps encore tiède.
Sans cette propriété, la vie aquatique aurait eu un tout autre destin. Dans un monde où la glace serait plus dense que l’eau, elle coulerait. Les lacs gèleraient par le fond. Chaque hiver aurait été une extinction massive pour les poissons et les plantes subaquatiques.

Une dépense d’énergie vertigineuse
Geler un lac demande une quantité d’énergie difficile à imaginer. Pour refroidir 1 gramme d’eau de 1 °C, il faut environ 4,18 joules. Pour transformer ce même gramme d’eau à 0 °C en glace, il faut 334 joules supplémentaires. Le changement d’état coûte bien plus cher que le simple refroidissement.
Prenons un exemple concret. Refroidir un très grand lac de 20 °C à 4 °C représente une énergie de l’ordre de 6 × 10¹⁸ joules. Cela correspond à la consommation électrique annuelle d’un pays entier. Former ensuite une couche de glace de 10 centimètres sur toute la surface nécessite encore environ 2 × 10¹⁶ joules.
Toute cette énergie est évacuée vers l’atmosphère, lentement, jour après jour. Le froid agit comme un aspirateur thermique, aspirant la chaleur du lac à travers sa surface.
Pourquoi une flaque gèle avant un grand lac ?
La vitesse de gel dépend de deux paramètres simples. La différence de température entre l’air et l’eau et la surface de contact.
Une petite flaque possède une grande surface par rapport à son volume. Elle perd rapidement sa chaleur. Une nuit froide suffit à la transformer en patinoire miniature. Un lac profond, lui, contient une masse d’eau énorme sous une surface relativement limitée. Le refroidissement prend du temps.
C’est la même logique qu’un café brûlant. Dans une soucoupe, il refroidit vite. Dans un thermos, il reste chaud longtemps.
Cette relation surface-volume explique pourquoi les grands lacs demandent plusieurs semaines de froid continu pour geler entièrement, là où un étang peu profond peut céder en quelques jours.
Les rives, premières victimes du gel
Le gel ne commence jamais au hasard. Il débute presque toujours sur les bords.
Près des rives, la profondeur est faible. Pour une même surface exposée à l’air froid, le volume d’eau à refroidir est plus petit qu’au centre. L’énergie perdue par mètre carré est identique. Le refroidissement est donc plus rapide là où l’eau est peu profonde.
À l’inverse, un lac dégèle souvent par le milieu car l’eau profonde, comme nous l’avons vu, y reste proche de 4 °C, ce qui constitue une réserve de chaleur importante sous la glace.
Cette chaleur remonte lentement et fragilise la glace par le dessous, tandis que le soleil l’attaque par le dessus.
Près des rives, l’eau est plus froide et moins abondante, la glace y résiste donc plus longtemps.
Ainsi, vous avez désormais pourquoi mon Lac de Créteil était encore gelé sur ses rives et non en son centre quand je suis allé à sa rencontre ce 07 janvier 2026 !
En résumé :
Sources :
- Wetzel, R. G., Limnology: Lake and River Ecosystems, Academic Press
Ouvrage de référence international sur la physique et l’écologie des lacs, détaillant la stratification thermique, l’anomalie de densité de l’eau et les mécanismes de gel hivernal. - US Geological Survey (USGS), Why does ice form on lakes and ponds before the water freezes solid?
Ressource pédagogique de référence expliquant clairement le rôle de l’anomalie de densité de l’eau et les échanges thermiques air–eau dans le gel des plans d’eau. - Encyclopaedia Britannica, entrées Density anomaly of water et Lake stratification
Synthèse scientifique rigoureuse sur les propriétés physiques de l’eau et leur impact sur le comportement thermique des lacs.